réponse simple
Réponse simple :
Au sein de certaines molécules, il y a des atomes chargés négativement et d'autres positivement1. C'est le cas par exemple de l'eau.
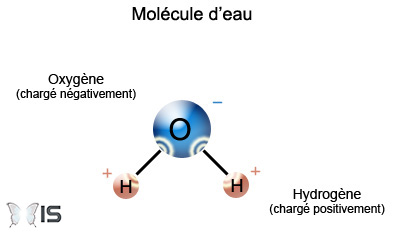
Structure d'une molécule d'eau
Il se trouve que les molécules de sel possèdent également des atomes chargés.
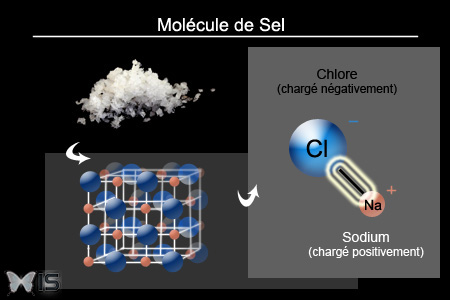
Structure chimique du sel
Lorsqu'on ajoute du sel dans l'eau, les molécules d'eau vont être attirées par les charges du produit et se regrouperont alors autour de lui.
Elles s'infiltrent ensuite entre les molécules du composé, ce qui a pour effet de les séparer les unes des autres. On appelle ce phénomène la dissolution2.
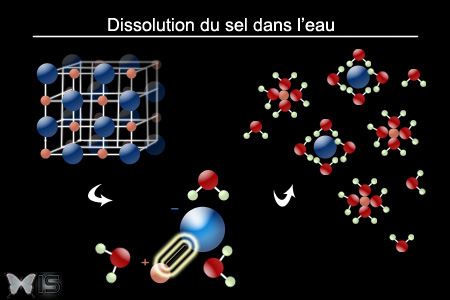
Dissolution du sel dans l'eau
Animation de dissolution du sel (© IS)
réponse avancée
Réponse avancée :
On a pour habitude de classer les liaisons chimiques selon la différence d'électronégativité des atomes. Celles qui possèdent la valeur la plus faible sont dites covalentes, puis polaires et finalement ioniques lorsque les électrons sont localisés sur un seul des atomes1.
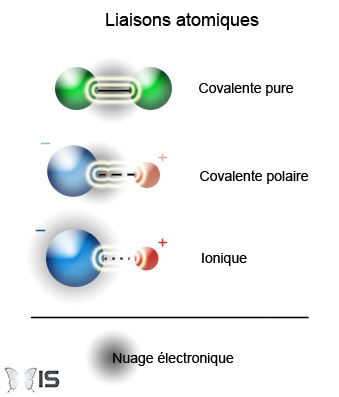
Les types primaires de liaisons chimiques
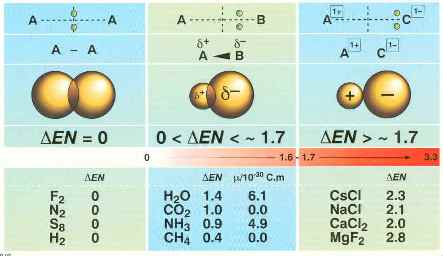
Les principales liaisons selon la différence d'électronégativité (source)
L'eau est par exemple un composé polaire et le sel est ionique.


Structure chimique de l'eau et du sel
Lorsqu'on mélange ces deux produits, les molécules d'eau et de sel sont mutuellement attirées par leurs charges partielles et forment de petits groupes.
Comme la liaison entre les deux atomes du sel est ionique, les électrons sont totalement localisés sur un seul des ions. Cette absence d'électrons entre les deux atomes permet donc à l'eau de s'infiltrer entre eux et de les isoler, phénomène que l'on nomme dissolution, ou encore solvatation2.

Solvatation du sel
Animation de dissolution du sel (© IS)
L'ajout d'énergie, par chauffage ou brassage, accélère considérablement la vitesse de dissolution en augmentant l'énergie cinétique des particules.





 / 70 votes
/ 70 votes

Commentaires
Bonjour Chahra,
Il me semble que les adoucisseurs d’eau à résine fonctionnent sur le même principe :
1. On implante dans la résine des zones chargées négativement où l’on place des ions sodium (Na+, un composé du sel de cuisine),
2. On met cette résine dans l’eau à adoucir,
3. Les ions calcium présents dans l’eau (Ca+) vont être attirés par les complexes chargés de la résine et remplacer ainsi certains des ions sodium,
4. L’eau devient plus concentrée en sodium (le nombre de Na+ « en liberté » augmente), mais sa dureté diminue (le nombre de Ca+ « en liberté » est réduite).
Donc oui, c’est bien la polarité des molécules (charges contraires) qui permet à cet échange d’avoir lieu. Vous pouvez lire cet article pour plus de détails, mais il est assez technique : udppc.asso.fr/.../...
Et voici une image chimique du remplacement des ions (= molécules chargées) : en.wikipedia.org/.../...
Mais il existe d’autres systèmes d’adoucisseurs d’eau qui ne procèdent pas de la même manière, comme par exemple ceux à CO2 : fr.wikipedia.org/.../...'eau#Fonctionnement_d.27un_adoucisseur_au_CO2.5Br.C3.A9f..C2.A0n.C3.A9cessaire.5D
Une bonne fin de semaine à vous.